Chapitre 10 – Hypertrophie bénigne de la prostate
Auteurs : Thomas Seisen, Evanguelos Xylinas |
Relecture : Morgan Rouprêt, Grégoire Robert |
Plan |
Objectifs pédagogiques
|
Résumé
L’hypertrophie bénigne de la prostate (HBP) est une pathologie fréquente favorisée par le vieillissement et liée au développement d’un adénome prostatique responsable d’un obstacle chronique à la vidange vésicale. L’évolution de l’HBP peut entraîner un retentissement sur :
- le bas appareil urinaire : vessie de lutte ;
- le haut appareil urinaire : insuffisance rénale chronique obstructive.
Le diagnostic clinique repose sur l’interrogatoire et la recherche des symptômes urinaires du bas appareil (SBAU) qui sont des signes fonctionnels urinaires :
- retard au démarrage, dysurie, jet faible, gouttes retardataires ;
- pollakiurie, urgenturie, impériosité, brûlures mictionnelles.
Le toucher rectal (TR) retrouve une prostate volumineuse (> 20 g), ferme, indolore, lisse, régulière, avec disparition du sillon médian. Il permet également de dépister un cancer de la prostate. Un TR évocateur d’un cancer de la prostate est une indication à réaliser des biopsies prostatiques avec examen anatomopathologique quel que soit le PSA.
Les complications aiguës sont la rétention aiguë d’urine, les infections urogénitales, l’hématurie et l’insuffisance rénale aiguë obstructive.
Les complications chroniques sont la rétention vésicale chronique, la lithiase vésicale et l’insuffisance rénale chronique obstructive.
Les examens complémentaires de première intention à demander pour le bilan d’une HBP sont : PSA, créatinine, ECBU, débitmétrie, échographie réno-vésico-prostatique. Malgré l’augmentation du PSA avec le volume prostatique, un taux de PSA > 4 ng/mL est une indication à réaliser des biopsies prostatiques avec examen anatomopathologique.
Les indications des trois traitements de l’HBP sont résumées dans le tableau 10.6.
| Abstention/surveillance | Traitement médical | Traitement chirurgical | |
|---|---|---|---|
| Indications | – HBP non compliquée – SBAU minimes/modérés sans altération de la qualité de vie |
– HBP non compliquée – SBAU minimes/modérés avec altération de la qualité de vie |
– HBP compliquée – SBAU modérés/sévères résistant au traitement médical – Ou préférence du patient |
Le traitement médical de l’HBP comprend les classes thérapeutiques suivantes : ?-bloquants, IPDE5, inhibiteurs de la 5?-réductase et phytothérapie. Les ?-bloquants sont efficaces après 48 heures de traitement et sont responsables d’hypotension orthostatique, alors que les inhibiteurs de la 5?-réductase sont efficaces après 6 mois de traitement et ont pour conséquence de diviser par 2 le taux de PSA.
Le traitement chirurgical comprend trois interventions : l’incision cervico-prostatique (ICP), la résection transurétrale de prostate (RTUP) et l’adénomectomie voie haute (AVH). Après RTUP ou AVH, l’adénome prostatique doit être envoyé en anatomopathologie à la recherche d’un cancer de la prostate. Le principal effet secondaire est l’éjaculation rétrograde.
Le suivi d’un patient présentant une HBP se fait sur le score IPSS, la débitmétrie et la mesure du résidu post-mictionnel annuel. Le dépistage du cancer de la prostate par le TR et un PSA annuel est recommandé chez les patients de 50 à 75 ans ou à partir de 45 ans en cas de facteurs de risque (origine afro-antillaise, antécédents familiaux).
I – Pour comprendre
L’hypertrophie bénigne de la prostate (HBP) constitue un obstacle sous-vésical à l’écoulement des urines (signes obstructifs) et peut entraîner une réaction de la paroi vésicale (hyperactivité vésicale).
L’HBP est une affection bénigne fréquente occasionnant des symptômes urinaires du bas appareil (SBAU) altérant la qualité de vie et pouvant être à l’origine de complications potentiellement graves. Elle correspond à une hyperplasie des glandes de la prostate péri-urétrale (zone de transition de la prostate).
La symptomatologie peut être stable ou s’aggraver plus ou moins rapidement.
Cependant, il n’existe pas de parallélisme entre le volume d’une HBP et la gravité des SBAU.
II – Physiopathologie
L’HBP est une affection :
- bénigne ;
- très fréquente ;
- liée au vieillissement.
L’HBP correspond à une hyperplasie de la zone de transition de la prostate entourant l’urètre sous-vésical (fig. 10.1). L’adénome prostatique se développe classiquement à partir des lobes droit et gauche de la prostate mais peut parfois affecter un troisième lobe dit « lobe médian » situé à la face postérieure du col vésical. L’adénome peut ainsi être responsable d’un obstacle chronique à la vidange vésicale avec un risque de retentissement sur :
- le bas appareil urinaire : vessie de lutte ;
- le haut appareil urinaire : insuffisance rénale chronique obstructive.
 |
La vessie de lutte est caractérisée par une hypertrophie détrusorienne puis l’apparition de trabéculations et de diverticules vésicaux. Au stade ultime, lorsque la vessie est distendue et non fonctionnelle, elle est responsable d’une rétention chronique avec miction par regorgement. Une insuffisance rénale chronique obstructive liée au reflux et à la dilatation bilatérale des cavités pyélocalicielles peut alors apparaître.
Cependant, il n’existe pas de parallélisme anatomoclinique : les symptômes urinaires et le retentissement de l’HBP ne sont pas proportionnels au volume de l’adénome prostatique.
L’évolution d’un adénome prostatique ne se fait pas systématiquement vers l’apparition de complications. L’HBP peut être latente et responsable uniquement d’une gêne fonctionnelle. L’HBP ne dégénère jamais en cancer de la prostate mais ces deux pathologies sont favorisées par le vieillissement, et surviennent sur le même terrain. Le cancer de la prostate, développé à partir de la zone périphérique de la prostate, est donc souvent recherché lors du diagnostic d’une HBP.
III – Facteurs de risque d’HBP
L’HBP est multifactorielle. Les deux principaux facteurs de risque de l’HBP sont l’âge et le statut hormonal du patient.
Certains facteurs de progression de l’HBP (apparition de signes cliniques) ont été identifiés, et notamment l’âge, le taux de PSA sérique et le volume de la prostate.
IV – Critères diagnostiques cliniques de l’HBP
A – Symptômes du bas appareil urinaire (SBAU)
L’HBP est à l’origine de SBAU. Il s’agit de signes fonctionnels urinaires qui peuvent être stratifiés en SBAU de la phase de remplissage, de la phase mictionnelle et de la phase postmictionnelle (AFU 2014) (tableau 10.1).
| Phase de remplissage | Phase mictionnelle | Phase post-mictionnelle |
|---|---|---|
| * International Continence Society. Traduction par le Comité des troubles mictionnels de l’homme de l’Association française d’urologie. | ||
| Pollakiurie diurne et nocturne, urgenturie, nycturie | Retard au démarrage, dysurie, jet faible, interruption de la miction jet haché, miction par poussée | Gouttes retardataires, sensation de vidange vésicale incomplète |
La sévérité et le retentissement des signes fonctionnels urinaires de l’HBP sont évalués par le score IPSS (International Prostate Symptom Score). Les SBAU sont souvent responsables d’une altération de la qualité de vie.
L’association de SBAU avec une dysfonction sexuelle est fréquente. Par conséquent, l’évaluation de la fonction sexuelle, notamment par un questionnaire, est recommandée dans le bilan initial de l’HBP.
B – Toucher rectal (TR)
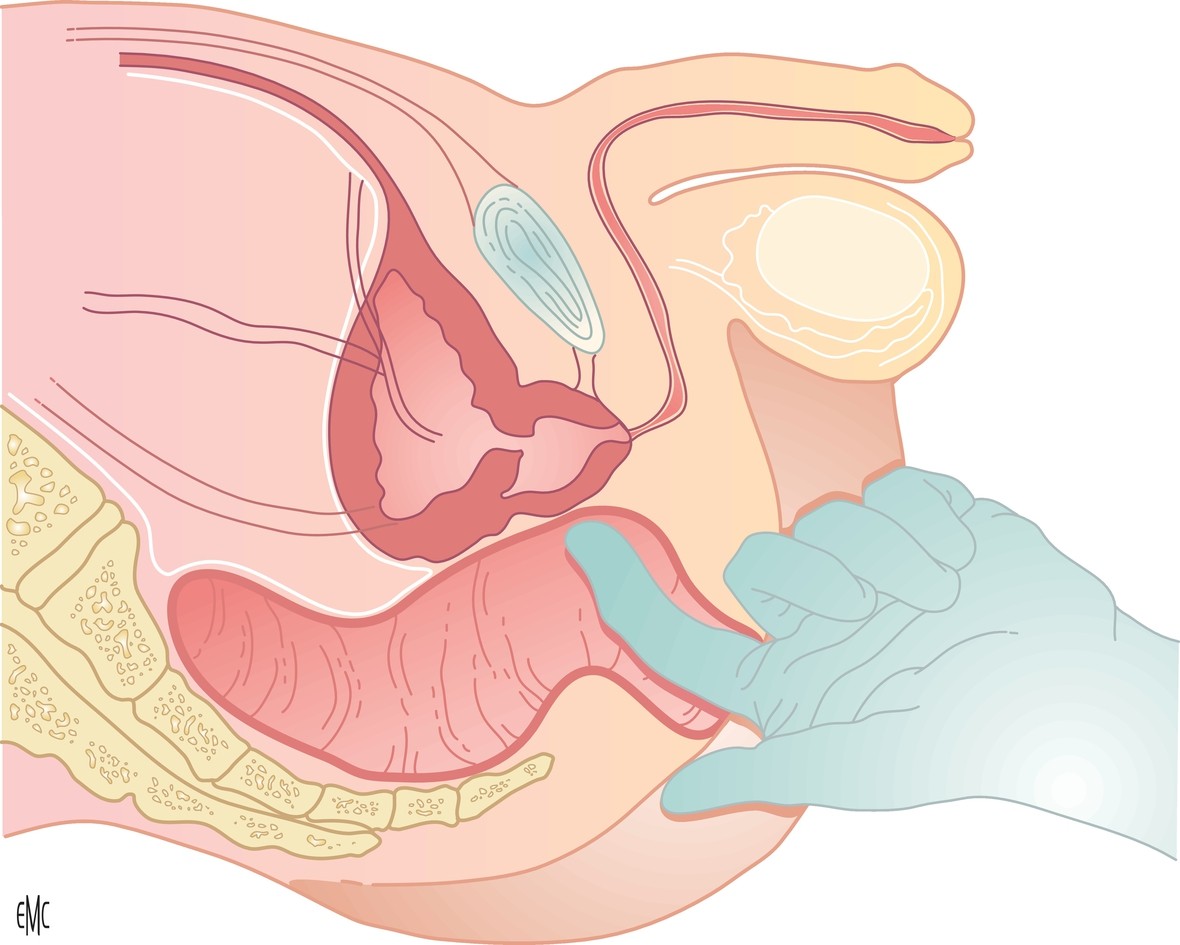
Le toucher rectal est systématiquement réalisé (fig. 10.2). Il permet de diagnostiquer l’HBP et de dépister un éventuel cancer de la prostate associé au sein de la même glande.
En cas d’HBP, le toucher rectal va identifier certaines particularités de la prostate : la glande est augmentée de volume (> 20 g), elle est souple, indolore, lisse, régulière et s’accompagne d’une disparition du sillon médian.
Un toucher rectal évocateur d’un cancer de la prostate (nodule dur, asymétrie de la prostate, ) est une indication à réaliser desbiopsies prostatiques avec examen anatomopathologique quel que soit le taux de PSA.
| Source : Bastien L, Fourcade RO , Makhoul B, Meria P, Desgrandchamps F. Hyperplasie bénigne de la prostate. EMC – Urologie 2011 : 113 [Article 18-550-A-10]. © 2011 Elsevier Masson SAS. Tous droits réservés. |
 |
Recommandations AFU 2014/EAU 2014
Le diagnostic clinique de l’HBP repose sur :
- l’interrogatoire : dépistage et évolution des SBAU, score IPSS, dépistage d’une dysfonction sexuelle associée ;
- l’examen physique : TR.
V – Complications aiguës
A – Rétention aiguë d’urine (RAU)
Il existe un globe vésical aigu douloureux, d’apparition brutale, caractérisé par une envie impérieuse d’uriner.
Le traitement est le drainage vésical des urines en urgence par la mise en place d’une sonde vésicale ou d’un cathéter sus-pubien.
B – Infections
L’HBP favorise la survenue d’infections urogénitales telles que la prostatite et l’orchi-épididymite.
C – Hématurie
Il s’agit habituellement d’une hématurie macroscopique initiale (liée à la rupture de petites varices prostatiques). L’HBP ne peut être rendue responsable d’une hématurie qu’après avoir éliminé les autres étiologies d’hématurie macroscopique (tumeur du rein ou de la vessie, calculs urinaires, infections, ).
D – Insuffisance rénale aiguë obstructive
En présence d’une insuffisance rénale aiguë, il faut éliminer une rétention aiguë d’urine favorisée par l’HBP.
VI – Complications chroniques
A – Rétention vésicale chronique
Il existe un globe vésical chronique qui est le plus souvent indolore, sans besoin d’uriner exprimé par le patient, responsable de mictions ou d’incontinence urinaire par regorgement (« trop plein d’urine »).
B – Lithiase vésicale de stase
La stase chronique des urines dans la vessie peut entraîner la constitution de calculs vésicaux responsables d’épisodes d’hématurie ou d’infections urinaires à répétition. L’ASP et l’échographie retrouvent des images calciques intravésicales de taille variable (fig. 10.3A et 10.3B). La lithiase vésicale est toujours le symptôme d’une difficulté de vidange de la vessie (lithiase d’organe) par opposition aux lithiases rénales qui sont le plus souvent témoin d’un désordre métabolique (lithiases d’organisme).
 |
C – Insuffisance rénale chronique obstructive
La dilatation bilatérale des cavités pyélocalicielles est chronique et indolore. L’urétérohydronéphrose est responsable d’un amincissement du parenchyme rénal et d’une insuffisance rénale chronique obstructive.
Les complications aiguës et chroniques sont résumées dans le tableau 10.2.
| Complications aiguës | Complications chroniques | |
|---|---|---|
| Bas appareil urinaire | Rétention aiguë d’urine Hématurie Infection |
Rétention vésicale chronique Lithiase vésicale de stase |
| Haut appareil urinaire | Insuffisance rénale aiguë obstructive | Insuffisance rénale chronique obstructive |
VII – Diagnostic différentiel
Les SBAU sont des symptômes aspécifiques et peuvent être également présents au cours de nombreuses pathologies urologiques :
- vessie neurologique ;
- sténose de l’urètre d’origine infectieuse ou traumatique (AVP ± fracture du bassin, sondage traumatique) ;
- maladie du col vésical ;
- infections comme la prostatite chronique ;
- calculs urinaires ;
- tumeurs de la vessie caractérisées par la présence d’une hématurie.
Devant toute hématurie macroscopique, ou en cas de symptômes prédominants d’hyperactivité de vessie, il faut éliminer une tumeur de la vessie par la réalisation d’une fibroscopie vésicale.
VIII – Examens complémentaires
A – ECBU
L’ECBU permet d’éliminer une infection urinaire responsable de SBAU identiques à ceux de l’HBP. En dehors de l’ECBU, aucun examen complémentaire n’est recommandé de façon systématique.
A – Taux de PSA
Le dosage du taux de PSA permet essentiellement de suspecter un cancer de la prostate associé à l’HBP.
Le PSA est un marqueur spécifique de la glande de la prostate mais certainement pas du cancer de la prostate. Il est donc possible d’observer une augmentation du PSA au-delà de 4 ng/mL en cas d’HBP associée. Schématiquement on peut retenir que 10 mL de volume prostatique peuvent augmenter le PSA de 1 ng/mL. À titre d’exemple un patient avec une prostate de 50 grammes peut avoir un PSA à 5 ng/mL (calcul de la densité de PSA). Cependant, de première intention, dans le cadre d’un diagnostic individuel précoce du cancer de la prostate, on proposera systématiquement des biopsies de prostate au-dessus de 4 ng/mL. Les autres facteurs favorisant l’augmentation du taux de PSA sont multiples : l’infection (prostatite), les biopsies prostatiques, l’éjaculation, l’âge, la race, le TR.
B – Créatinine
Le dosage de la créatinine permet d’évaluer le haut appareil urinaire et de dépister une insuffisance rénale chronique.
D – Débitmétrie
La débitmétrie permet d’objectiver et quantifier la dysurie. Pour pouvoir interpréter une débitmétrie, un volume uriné supérieur à 150 mL est nécessaire. Les paramètres étudiés au cours de la débitmétrie sont : le volume uriné, le débit maximal, le débit moyen, et le temps mictionnel.
Une courbe normale présente une forme en cloche avec un débit maximal entre 20 et 30 mL/s alors qu’une courbe aplatie est caractéristique de l’obstruction liée à l’HBP (fig. 10.4). La dysurie est considérée comme importante pour un débit maximal inférieur à 10 mL/s.
 |
E – Échographie réno-vésico-prostatique
L’échographie rénale évalue le retentissement sur le haut appareil urinaire. Elle recherche une dilatation bilatérale des cavités pyélocalicielles, un amincissement du parenchyme rénal et une dé-différenciation cortico-médullaire.
L’échographie vésicale évalue le retentissement sur le bas appareil urinaire. Elle recherche une hypertrophie détrusorienne, des diverticules vésicaux (fig. 10.5), une lithiase vésicale et un résidu post-mictionnel significatif.
L’échographie prostatique est réalisée par voie transrectale. Elle permet d’évaluer le volume prostatique et de rechercher un lobe médian.
| 1. Vessie. 2. Collet. 3. Diverticule. |
 |
F – Autres examens complémentaires
D’autres examens complémentaires peuvent être réalisés dans certaines indications particulières. Une fibroscopie vésicale est systématiquement réalisée en consultation si le patient présente des antécédents d’hématurie afin d’éliminer une tumeur vésicale. Un bilan urodynamique est indiqué en cas de doute diagnostique. Une UCRM peut être demandée à la recherche d’une sténose urétrale.
Recommandations AFU 2012/EAU 2015
Les examens complémentaires de première intention à demander pour le bilan d’une HBP sont :
- PSA ;
- créatinine ;
- ECBU ;
- débitmétrie ;
- échographie réno-vésico-prostatique.
IX – Traitement
Les différentes alternatives thérapeutiques dépendent de l’importance des SBAU, de l’apparition de complications, et de la préférence du patient. Ce dernier doit être informé des différentes options thérapeutiques et des avantages/inconvénients de chacune d’entre elles.
A – Abstention/surveillance
Recommandations AFU 2012/EAU 2015
Les indications de l’abstention/surveillance sont :
- HBP non compliquée ;
- SBAU minimes/modérés sans altération de la qualité de vie.
Le patient doit être éduqué, informé et rassuré sur le risque d’évolution de l’HBP. Certaines règles hygiéno-diététiquespeuvent être instaurées, notamment : la réduction des apports hydriques après 18 heures, la diminution de la consommation de caféine et d’alcool, le traitement d’une constipation associée et enfin l’arrêt des traitements favorisant la dysurie (anticholinergiques, neuroleptiques ).
B – Traitement médical
Recommandations AFU 2012/EAU 2015
Les indications du traitement médical sont :
- HBP non compliquée et sbau modérés/sévères avec altération de la qualité de vie.
Le patient est candidat à un traitement médical symptomatique de l’HBP. L’objectif principal est d’améliorer la qualité de vie des patients. Il existe quatre classes thérapeutiques (tableau 10.3).
| ?-bloquants | Inhibiteurs de la 5?-réductase | Phytothérapie | IPDE5 | |
|---|---|---|---|---|
| Action pharmacologique | Diminution du tonus de l’urètre postérieur après 48 h de traitement | Diminution du volume prostatique après 6 mois de traitement | Mal connu | Non élucidé |
| Effets secondaires | – Hypotension orthostatique– Céphalées, vertiges – Troubles de l’accommodation – Éjaculation rétrograde |
– Troubles de l’érection – Diminution de la libido – Gynécomastie |
– Aucun | – Hypotension artérielle etcollapsus en cas de prise de dérivés nitrés concomitante (contre-indication) |
| Exemples | – Alfusozine (Xatral®) – Tamsulosine (Josir®, Omix®) – Silodosine (Urorec®) |
– Finastéride (Chibroproscar®) – Dutastéride (Avodart®) |
– Serenoa Repens (Permixon®) – Pygeum Africanum (Tadenan®) |
– Tadafil (Cialis®) quotidien Non remboursé seul médicament disponible |
Les ?-bloquants doivent être prescrits avec précaution chez les patients âgés, coronariens, et en cas de traitement antihypertenseur associé.
Les inhibiteurs de la 5?-réductase doivent être prescrits préférentiellement chez les patients présentant une prostate > 40 g. Ils ont pour conséquence de diminuer le taux de PSA de 50 %. Le dépistage du cancer de la prostate chez les patients traités par inhibiteurs de la 5?-réductase nécessite de multiplier par 2 le taux de PSA.
En cas d’inefficacité d’un médicament seul, il est possible d’associer un ?-bloquant et un inhibiteur de la 5?-réductase et d’instaurer ainsi une bithérapie. Cependant, les effets secondaires des différentes classes thérapeutiques se cumulent les uns aux autres.
C – Traitement chirurgical
Recommandations AFU 2012/EAU 2015
Les indications du traitement chirurgical sont :
- HBP compliquée (RAU, calcul ou diverticule vésical, IRC obstructive ) ;
- ou SBAU modérés/sévères résistant au traitement médical ;
- ou préférence du patient.
Il s’agit du seul traitement curatif de l’HBP. L’objectif principal est d’améliorer la qualité de vie des patients en réalisant l’exérèse de l’adénome. Un cancer de la prostate peut donc toujours se développer à partir de la zone périphérique laissée en place. Il existe trois interventions (tableau 10.4, fig. 10.6).
| Incision cervico-prostatique (ICP) | Résection transurétrale de prostate (RTUP) | Adénomectomie voie haute (AVH) | |
|---|---|---|---|
| Indication | Prostate < 30 g | Prostate < 80 g | Prostate > 80 g |
| Voie d’abord | Endoscopie | Endoscopie | Laparotomie |
| Technique | Incision du col vésical et de l’adénome prostatique (fig. 10.6A) | Résection en copeaux de l’adénome prostatique (fig. 10.6B) | Énucléation de l’adénome prostatique (fig. 10.6C) |
| Complications aiguës | – Hématurie, RAU – Infection urinaire |
– Hématurie, RAU – Infection urinaire – TURP syndrome (hyponatrémie) |
– Hématurie, RAU – Infection urinaire – Hématome, abcès de paroi |
| Complications chroniques | – Éjaculation rétrograde – Sténose du col vésical/urètre |
– Éjaculation rétrograde – Sténose du col vésical/urètre |
– Éjaculation rétrograde – Sténose du col vésical/urètre |
NB : autre alternative chirurgicale : la photovaporisation de l’HBP à l’aide d’un laser Greenlight® ou la résection laser (HOLEP) qui sont en cours d’évaluation (avantages : pas de TURP syndrome et faisabilité sans arrêt des anticoagulants). À noter également l’utilisation possible de la radiofréquence (Prostiva®) dont l’efficacité est entre les traitements médicaux et les traitements chirurgicaux ablatifs. L’avantage principal est l’absence d’éjaculation rétrograde, l’inconvénient la nécessité de refaire souvent un traitement (tous les 3 à 5 ans).
| A. ICP. Incision du col vésical et de l’adénome en partant de l’orifice urétéral droit. B. RTUP. (1. Lumière. 2. Courant électrique. 3. Irrigation. 4. Gaine). C. AVH. (1. Vessie. 2. Adénome. 3. Rectum). |
 |
Une intervention chirurgicale pour HBP nécessite un ECBU négatif. Après résection ou énucléation, l’adénome prostatique doit être envoyé en anatomopathologie à la recherche d’un cancer de la prostate.
Le TURP syndrome ou syndrome de réabsorption du liquide d’irrigation est une complication peropératoire rare de la RTUP en rapport avec un important passage de liquide d’irrigation sucré et hypotonique (glycocolle) dans la circulation générale. Ce syndrome débute au bloc opératoire et associe chez un patient sous rachianesthésie des troubles visuels (mouches volantes), des céphalées, une hypotension, une bradycardie et des douleurs thoraciques. Ces signes sont en rapport avec unesurcharge volémique et une hyponatrémie de dilution. Les facteurs de risque sont le saignement peropératoire abondant et une durée opératoire supérieure à 60 minutes.
Le traitement du TURP syndrome dépend de la natrémie :
- hyponatrémie modérée (> 120 mmol/L) : restriction hydrique associée un diurétique ;
- hyponatrémie sévère (< 120 mmol/L) : sérum physiologique hypertonique en perfusion lente (risque de myélinolyse centropontine).
Le principal effet secondaire du traitement chirurgical de l’HBP est l’éjaculation rétrograde. Le risque varie en fonction de l’intervention : AVH > RTUP > ICP. Contrairement à la prostatectomie totale indiquée pour le traitement d’un cancer de la prostate, les risques de dysfonction érectile et d’incontinence urinaire sont faibles.
D – Traitement palliatif
Les patients présentant une contre-indication opératoire peuvent être traités soit par la pose d’une sonde vésicale ou d’uncathéter sus-pubien à demeure, soit par une endoprothèse urétrale, soit par les auto-sondages.
L’arbre décisionnel de la prise en charge chirurgicale de l’HBP est présenté dans la figure 10.7.
 |
X – Surveillance
Recommandations AFU 2012/EAU 2015
Le suivi d’un patient présentant une HBP se fait à l’aide de :
- l’interrogatoire avec score IPSS ;
- la débitmétrie ;
- la mesure du résidu post-mictionnel.
Le dépistage du cancer de la prostate par le TR et un PSA annuel est recommandé chez les patients de 50 à 75 ans ou à partir de 45 ans en cas de facteurs de risque (origine afro-antillaise, antécédents familiaux).
Le rythme de la surveillance dépend du traitement instauré (tableau 10.5).
| Abstention/surveillance | Traitement médical ?-bloquants |
Traitement médical inhibiteurs de la 5?-réductase |
Traitement chirurgical | |
|---|---|---|---|---|
| Rythme | À 6 mois puis annuel | À 6 semaines, 6 mois puis annuel | À 12 semaines, 6 mois puis annuel | À 6 semaines, 3 mois puis annuel |
Après l’introduction des ?-bloquants ou des inhibiteurs de la 5?-réductase, les patients doivent être revus précocement pour évaluer l’efficacité du traitement médical.
Après traitement chirurgical, les patients sont revus à 6 semaines pour vérifier l’absence de complications et être informés des résultats anatomopathologiques. L’efficacité du traitement ne peut être évaluée qu’à partir de 3 mois.
Pour en savoir plus
- Recommandations AFU. 2015. www.urofrance.org
- Recommandations de l’European Association of Urology (EAU) 2015. http://uroweb.org/guideline/treatment-of-non-neurogenic-male-luts/
Vous pourrez également aimer
Continuer votre lecture
- Chapitre 14 – Hématurie
- Chapitre 12 – Infections sexuellement transmissibles
- Chapitre 13 – Transplantation d’organes
- Chapitre 11 – Infections urinaires de l’enfant et de l’adulte
- Chapitre 09 – Trouble de l’érection
- Chapitre 08 – Troubles de la miction de l’adulte et du sujet âgé
- Chapitre 06 – Andropause
- Chapitre 07 – Incontinence urinaire de l’adulte et du sujet âgé










